La recherche en fibrose kystique 2017
L’année 2017 a été l’année de tous les espoirs pour l’ensemble des personnes atteintes de fibrose kystique.
Les avancées en recherche et en clinique ont été résumées dans la session plénière du congrès Nord Américain de la fibrose kystique tenu du 2 au 4 novembre 2017 à Indianapolis, aux États-Unis.
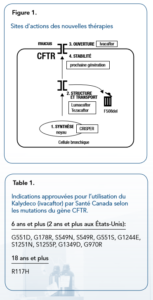
Deux médicaments sont maintenant approuvés par Santé Canada pour le traitement des personnes atteintes de fibrose kystique et ayant des mutations spécifiques. Il s’agit de l’ivacaftor (nom commercial, Kalydeco) et de la combinaison d’ivacaftor et de lumacaftor (Orkambi). Il existe plusieurs classes de mutaitons du gène CFTR (Cystic fibrosis transmembrane conductance regulator) mais les classes 1, 2 et 3 sont associées à la majorité des manifestations clinique de la maladie (Figure 1). Les mutations de classe III empêchent l’ouverture du canal de transport des ions chlorure dans les cellules affectées. L’utilisation de l’ivacaftor chez les personnes atteintes de mutations spécifiques, surtout de classe III (table 1) donne des améliorations cliniques remarquables. Il s’agit d’une percée scientifique majeure qui démontre la possibilité de corriger le défaut à la base de la FK en donnant un simple comprimé par voie orale. Malheureusement moins de 2 % des personnes atteintes de FK au Québec ont ces mutations, ce qui limite sévèrement l’utilisation de l’ivacaftor. Par contre, près de 89 % des personnes atteintes de FK au Québec ont au moins une copie de la mutation de classe II, le F508del, et 50 % en ont 2 copies (ie: ils sont homozygotes pour cette mutation). Une mutation de classe II ne permet pas à la protéine CFTR de se rendre à la membrane cellulaire pour faciliter le transport des ions de chlorure. Plusieurs études clinques ont démontré des bienfaits modestes du traitement d’Orkambi chez les patients ayants 2 copies de F508del, mais aucun effet bénéfique n’a été noté chez les patients ayant une seule copie de la mutation. Bien que modestes, ces améliorations de la fonction du CFTR donnent de l’espoir aux personnes affectées par la FK, et une demande d’inscription du Orkambi aux listes des médicaments remboursés par le régime d’assurance publique du Québec a été déposée.
À la suite de l’avis émis par les membres du comité de l’évaluation des médicaments aux fins d’inscription aux listes des médicaments, l’Institut national d’excellence en santé et en service sociaux (INESSS) a recommandé au ministre de ne pas inscrire Orkambi au Québec pour le traitement de la fibrose kystique chez les individus homozygotes pour la mutation F508del du gène CFTR. L’INESSS indique ne pas reconnaître une valeur thérapeutique suffisante qui pourrait justifier son inscription. Il ne s’agit pas d’une décision qui fait l’unanimité parmi les cliniciens experts en FK au Québec et ailleurs. Par contre, il est possible d’obtenir le remboursement de Orkambi par le programme de patients d’exception de la régie de l’assurance maladie du Québec chez des personnes qui répondent à certains critères. Afin d’être éligible au remboursement, il faut avoir 2 mutations F508del, bénéficier d’un régime thérapeutique optimal pour contrer la FK, et surtout, démontrer une adhérence exemplaire au plan thérapeutique. Ce dernier critère est essentiel non seulement pour obtenir le remboursement d’Orkambi, mais surtout pour assurer la meilleure évolution aux personnes atteintes de la FK.
L’efficacité des médicaments disponibles pour le traitement des patients porteurs d’au moins une mutation de type F508del du gène CFTR est limitée par le fait que cette mutation est liée à 3 défauts de la protéine. Idéalement un médicament devra corriger chacun de ces défauts sinon il faudra combiner 3 médicaments.
Les 3 défauts sont les suivants: 1. la protéine CFTR F508del est mal formée et elle est donc détruite avant de se rendre à la membrane des cellules où elle doit normalement faciliter le passage des ions de chlorure, 2. une fois rendue à la membrane, le CFTR F508del reste fermé et ne laisse pas passer les ions, et 3. La protéine F508del qui se rend à la membrane est instable et elle est retirée de la membrane par des mécanismes de contrôle de la qualité des protéines. Les deux premiers défauts sont corrigés par l’ivacaftor et le lumacaftor (les 2 composantes du Orkambi). Par contre, aucun médicament sur le marché ne stabilise la protéine CFTR F508del une fois qu’elle est rendue à la membrane. Ceci est en train de changer. Des chercheurs ont découvert une nouvelle catégorie de molécules appelées les correcteurs de la prochaine génération (« nextgen correctors »), qui augmentent grandement la stabilité du CFTR F508del à la membrane cellulaire et augmentent beaucoup l’efficacité des autres agents tels que l’ivacaftor et le lumacaftor. Une triple combinaison de médicaments pourrait donc être une solution pour les individus atteints de FK et porteurs d’au moins une mutation CFTR F508del.
Lorsqu’on consomme plus d’un médicament à la fois, il risque toujours d’y avoir des interactions néfastes entres les médicaments. Le lumacaftor est métabolisé par le foie, et il est particulièrement susceptible d’induire des interactions indésirables avec les autres médicaments. C’est pourquoi une alternative moins propice aux interactions est recherchée pour remplacer le lumacaftor et permettre l’ajout d’un correcteur de prochaine génération. Un pas important dans cette direction vient d’être franchi. La compagnie Vertex a récemment terminé une vaste étude qui a démontré que le tezacaftor a une efficacité équivalente au lumacaftor mais, avec nettement moins de potentiel d’interactions avec les autres médicaments. Il s’agit d’une étape clé dans le développement de nouveaux médicaments qui pourrait aider la majorité des patients avec FK. Il reste maintenant à trouver un correcteur de la prochaine génération à ajouter à la combinaison d’ivacaftor et de tezacaftor. Cette dernière étape est en voie de résolution.
Des études in vitro ont permis aux chercheurs de découvrir plusieurs molécules de la prochaine génération des correcteurs et de démontrer une correction beaucoup plus importante de la fonction du CFTR F508del lorsqu’ajouté à la combinaison d’ivacaftor et de tezacaftor. Ces études encourageantes se traduisent maintenant par plusieurs études cliniques chez des patients porteurs d’une ou de deux mutations de F508del. Les résultats de ces études pourraient être connus d’ici un an et, ensuite, mener à la mise en marché d’une médication beaucoup plus efficace pour la majorité des individus atteints de FK.
Même si cette recherche excitante livre ses promesses, il restera environ 10 % des personnes atteintes de FK qui ne bénéficieront pas des ces avancées pharmacologiques. Par contre, un nouveau domaine de recherche connu sous le nom de la technologie “CRISPR/Cas9” offre beaucoup d’espoir. Il s’agit d’une façon d’effectuer une réparation spécifique d’un défaut génétique sans pour autant remplacer le gène. C’est un peu comme si on réparait une puce électronique de notre disque dur au lieu de remplacer le disque dur au complet. Cette technologie avance à grands pas et a démontré son efficacité dans plusieurs modèles chez les animaux. Un des défis reste la façon de transporter la machinerie correctrice à l’intérieur des noyaux où se trouve le bagage génétique, mais ce n’est qu’une question de temps avant que des solutions pratiques soient développées pour y arriver.
En résumé, il y a eu beaucoup de développements thérapeutiques en FK dans la dernière année avec des résultats spectaculaires. Il est maintenant permis à la majorité des patients atteints de FK d’espérer avoir accès un jour à une thérapie qui transformera leur vie. Par contre, d’ici là, il faudra surtout travailler fort pour conserver son état de santé ce qui passera nécessairement par une excellente adhérence aux bonnes habitudes de vie et aux traitements prescrits par les membres de son équipe FK soignante.
Dr André Cantin
Pneumologue Professeur titulaire
Service de pneumologie Centre hospitalier de l’Université de Sherbrooke
Sherbrooke (Québec) CanadaAdidas Performance